El calcio, un elemento químico esencial para la vida, es conocido por su papel en la salud de los huesos y dientes. Sin embargo, la relevancia del calcio va más allá de la biología humana y se extiende a una amplia gama de campos científicos.
La masa atómica del calcio es un concepto físico y químico que se refiere a la masa promedio de todos los isótopos de calcio que se encuentran en la naturaleza, ponderada por su abundancia relativa.
La masa atómica se expresa en unidades de masa atómica unificada (uma) o daltons (Da), y para el calcio, su masa atómica promedio es de aproximadamente 40.078 u.
Cálculo de la masa atómica del calcio
La masa atómica del calcio se calcula teniendo en cuenta la abundancia relativa de sus isótopos naturales.
El calcio tiene varios isótopos, siendo el más abundante el calcio-40 (Ca-40), que representa aproximadamente el 96% de todo el calcio natural. Además, el calcio-44 (Ca-44) es otro isótopo común, constituyendo aproximadamente el 2.1% del calcio natural. Otros isótopos de calcio, como el Ca-42 y el Ca-48, son menos abundantes y tienen un efecto menor en la masa atómica promedio.
El cálculo de la masa atómica se realiza multiplicando la masa de cada isótopo por su abundancia relativa y sumando los resultados. En el caso del calcio, esto da como resultado una masa atómica promedio de alrededor de 40.078 u.
Tabla con las masas atómicas de los isótopos de calcio
La siguiente tabla muestra la masa atómica de cada isótopo de calcio y el porcentaje de su composición isotópica.
|
Isótopo |
Masa atómica (Da) |
Abundancia isotópica (fracción de cantidad) |
|
40 Ca |
39.962 5909 (2) |
96.941% (156) |
|
42 Ca |
41.958 618 (1) |
0.647% (23) |
|
43 Ca |
42.958 766 (2) |
0.135% (10) |
|
44 Ca |
43.955 482 (2) |
2.086% (110) |
|
46 Ca |
45.953 69 (2) |
0.004% (3) |
|
48 Ca |
47.952 5229 (6) |
0.187% (21) |
Propiedades y características del calcio
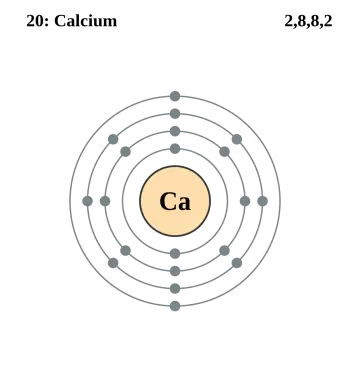
 El calcio (Ca) es un elemento químico de la tabla periódica con un número atómico de 20. Este número atómico indica que un átomo de calcio posee 20 protones en su núcleo y, en consecuencia, 20 electrones que orbitan a su alrededor.
El calcio (Ca) es un elemento químico de la tabla periódica con un número atómico de 20. Este número atómico indica que un átomo de calcio posee 20 protones en su núcleo y, en consecuencia, 20 electrones que orbitan a su alrededor.
La forma pura del calcio es un metal alcalinotérreo de color blanco plateado, conocido por su reactividad y su carácter blando. Fue en 1808 cuando Sir Humphry Davy logró aislarlo en su forma pura por primera vez.
Debido a su elevada actividad química, el calcio no se encuentra de manera libre en la naturaleza. Sin embargo, es posible obtener calcio metálico puro mediante el proceso de electrólisis de una masa fundida.
El calcio ocupa el quinto lugar en la lista de elementos más abundantes en la Tierra, después del oxígeno, el silicio, el aluminio y el hierro. Además, es un elemento que se encuentra en gran cantidad en el agua de mar, con una concentración aproximada de 400 mg/l. De hecho, constituye alrededor del 3,38% de la masa total de la corteza terrestre.
Este elemento químico pertenece al grupo de los metales alcalinotérreos y comparte su alta actividad química con otros miembros de este grupo de la tabla periódica. A pesar de su actividad, hay otros metales alcalinos que son aún más reactivos.
En la naturaleza, el calcio se encuentra comúnmente asociado con dióxido de carbono, oxígeno y humedad presentes en el aire, lo que contribuye a su presencia en diversas formas y compuestos en nuestro entorno.
Importancia de la masa atómica del calcio
La masa atómica del calcio es un concepto de gran importancia en la química, la física y la biología. Esta magnitud no solo es esencial para la comprensión de las propiedades y el comportamiento del calcio en sí, sino que también tiene numerosas aplicaciones en distintos campos científicos.
- En química, la masa atómica del calcio se utiliza para calcular la masa molar de compuestos que contienen calcio. La masa molar es crucial para la formulación de sustancias y la comprensión de las proporciones en las reacciones químicas. Por ejemplo, en el carbonato de calcio (CaCO₃), la masa molar se calcula sumando la masa del calcio, el carbono y el oxígeno, lo que permite determinar la cantidad de sustancia presente en una muestra.
- En física nuclear, la masa atómica del calcio es fundamental para calcular la energía de enlace de los núcleos atómicos. La energía de enlace es necesaria para entender procesos como la fisión y la fusión nucleares, que son fundamentales tanto en aplicaciones energéticas como en la comprensión de la estructura de la materia.
- En astrofísica, la masa atómica del calcio es relevante en la nucleosíntesis estelar, donde se forman elementos más pesados a partir de elementos más ligeros en el interior de las estrellas. El calcio se produce en este proceso, y su masa atómica contribuye a explicar la abundancia de calcio en el universo y cómo se forman los elementos.
- En biología, el calcio es esencial para la salud de los seres vivos, incluyendo los seres humanos. La masa atómica del calcio es clave para calcular la cantidad de calcio necesaria en la dieta y comprender su papel en la formación de huesos, la transmisión de señales nerviosas y muchas otras funciones biológicas.


