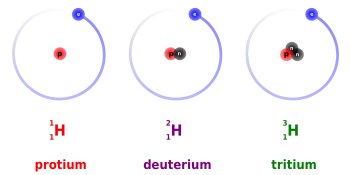
El tritio y el deuterio son dos de los tres isótopos de hidrógeno que se utilizan como combustible en las reacciones nucleares de fusión. El hidrógeno tiene tres isótopos: protio, deuterio y tritio.
Una reacción de fusión nuclear consiste en la unión de dos núcleos ligeros (átomos de hidrógeno) para formar uno solo. Esto ocurre cuando los núcleos se acercan tanto que las fuerzas nucleares entre ellos se vuelven muy fuertes.
Este tipo de energía está en fase de estudio y pretende ser una alternativa a los reactores de fisión nuclear actuales como fuente de energía eléctrica. La ventaja de esta tecnología es que producirá energía prácticamente ilimitada ya que el deuterio y el tritio se puede obtener del hidrógeno ordinario. Cabe recordar que este elemento químico se encuentra en abundancia en el aire y el agua de mar.
¿Qué es el tritio?
El tritio es un isótopo radiactivo del hidrógeno cuyo núcleo consiste en un protón y dos neutrones. La aplicación más importante del tritio es su utilización como combustible nuclear para la obtención de energía mediante la fusión nuclear.
Se suele designar mediante el símbolo T, aunque sistemáticamente se le debe simbolizar cómo 3H. Fue descubierto el 1934 por Rutherford, Oliphant y Harteck en el estudio del bombardeo del deuterio con deuterones.
El tritio es un isótopo natural que se genera por la acción de los rayos cósmicos sobre los gases atmosféricos. Por otro lado, este isótopo se puede obtener industrialmente por bombardeo de litio con neutrones de baja energía.
El tritio presenta una vida media de 12,3 años y emite radiación beta (β) de muy baja energía (0,018 MeV), totalmente libre de radiación γ, por lo que no presenta prácticamente radiotoxicidad.
Efectos del Tritio sobre la salud
Las partículas beta formadas por la reacción de descomposición del tritio se propagan en el aire solo 6,0 mm y ni siquiera pueden superar la capa superior de la piel humana. Sin embargo, este isótopo presenta un peligro de radiación cuando se inhala, se absorbe con los alimentos y se absorbe a través de la piel.
¿Para qué se utiliza el Tritio?
El tritio se puede utilizar en diferentes aplicaciones con diferentes objetivos:
-
Iluminación autoalimentada: las partículas beta emitidas por la desintegración radiactiva de pequeñas cantidades de tritio hacen que brillen sustancias químicas llamadas fósforos.
-
Armas nucleares: Este elemento químico se utiliza para mejorar la eficiencia y el rendimiento de las bombas de fisión nuclear y las etapas de fisión de las bombas de hidrógeno en un proceso conocido como refuerzo.
-
Fusión nuclear controlada: el tritio es un combustible importante para la fusión nuclear controlada en los diseños de reactores nucleares de fusión por confinamiento magnético y por inercia.
-
Química analítica: el tritio a veces se usa como radiomarcador. Tiene la ventaja de que casi todos los productos químicos orgánicos contienen hidrógeno, por lo que es fácil encontrar un lugar para colocar tritio en la molécula bajo investigación.
¿Qué es el deuterio?
El deuterio (²H), es un isótopo estable del hidrógeno que se encuentra en la naturaleza con una proporción de uno de cada 6500 átomos de hidrógeno. El núcleo atómico del deuterio está compuesto por un protón y un neutrón.
El deuterio también se le conoce por hidrógeno pesado y se representa con el símbolo ²H o como D. Aunque se trata de un átomo de hidrógeno, las propiedades físicas entre el deuterio y un átomo de hidrógeno ligero son máximas ya que la masa atómica del deuterio es el doble.
La Tierra y otras partes del Sistema Solar contiene deuterio. La fusión en las estrellas tiende a destruir el deuterio y, por otro lado, no hay procesos de creación naturales conocidos con excepción de la nucleosíntesis primordial.
¿Para qué sirve el Deuterio?
El deuterio se tutiliza en la energía nuclear como combustible en los procesos de fusión nuclear junto con el tritio. Su utilizació se explica por su gran sección eficaz de la reacción..
Por otra parte, en química este isótopo del hidrógeno se utiliza como trazalíneas isotópico no radiactivo en moléculas para estudiar cambios metabólicos y reacciones químicas porque desde un punto de vista químico se comporta de forma similar al hidrógeno ordinario.
