La química es una ciencia que se basa en la organización de los elementos químicos en la tabla periódica, una herramienta esencial para comprender y predecir el comportamiento de los átomos y las moléculas.
A lo largo de la historia, varios científicos contribuyeron al desarrollo de la tabla periódica, y uno de los primeros intentos de organizar los elementos fue la ley de las octavas de Newlands.
Orígenes históricos
 La ley de las octavas es un concepto que se originó a mediados del siglo XIX, cuando el químico británico John Newlands notó una tendencia en las propiedades químicas de los elementos.
La ley de las octavas es un concepto que se originó a mediados del siglo XIX, cuando el químico británico John Newlands notó una tendencia en las propiedades químicas de los elementos.
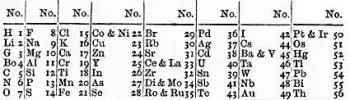
En 1864, Newlands propuso su idea en un artículo titulado "On the Law of Octaves" ("Sobre la ley de las octavas"). En este trabajo, Newlands observó que cuando los elementos se organizan en orden de sus masas atómicas crecientes, las propiedades químicas parecen repetirse cada ocho elementos.
Esta repetición se asemeja a la repetición de notas musicales en una octava musical, de ahí el nombre "ley de las octavas".
Limitaciones de la ley de las octavas de Newlands
Aunque la ley de las octavas fue un paso importante hacia la organización de los elementos, tenía limitaciones significativas.
La principal limitación era que solo funcionaba para algunos de los elementos conocidos en ese momento. En otras palabras, la ley no se aplicaba de manera consistente a todos los elementos. Newlands solo pudo aplicar su ley a los primeros 56 elementos de la tabla periódica, y después de eso, la repetición de propiedades químicas dejaba de ser evidente.
Además, Newlands también cometió errores en la organización de algunos elementos. Por ejemplo, colocó al hierro y al cobalto en la misma columna, aunque sus propiedades químicas son notablemente diferentes.
La tabla periódica de Mendeléyev: superando la ley de las octavas
A pesar de sus limitaciones, la ley de las octavas sentó las bases para la posterior creación de la tabla periódica moderna. El químico ruso Dmitri Mendeléyev, contemporáneo de Newlands, estaba trabajando en una organización similar de los elementos y desarrolló su propia versión de la tabla periódica en 1869.
La contribución más importante de Mendeléyev fue reconocer que la organización de los elementos debía basarse en sus masas atómicas, pero también debía tener en cuenta sus propiedades químicas y la periodicidad de estas propiedades.
Organización de la tabla de Mendeléyev
Mendeléyev organizó los elementos en función de su masa atómica creciente, pero dejó espacios vacíos en la tabla periódica donde creía que deberían estar elementos desconocidos en ese momento.
Lo sorprendente fue que las propiedades químicas de los elementos desconocidos encajaban perfectamente en las predicciones de Mendeléyev cuando se descubrieron posteriormente.
Osolescéncia de la ley de las octavas
El éxito de la tabla periódica de Mendeléyev y su capacidad para predecir las propiedades de elementos aún no descubiertos hizo que la ley de las octavas de Newlands quedara obsoleta y se considerara insuficiente para explicar la organización de los elementos.
La tabla periódica moderna y la organización de los elementos
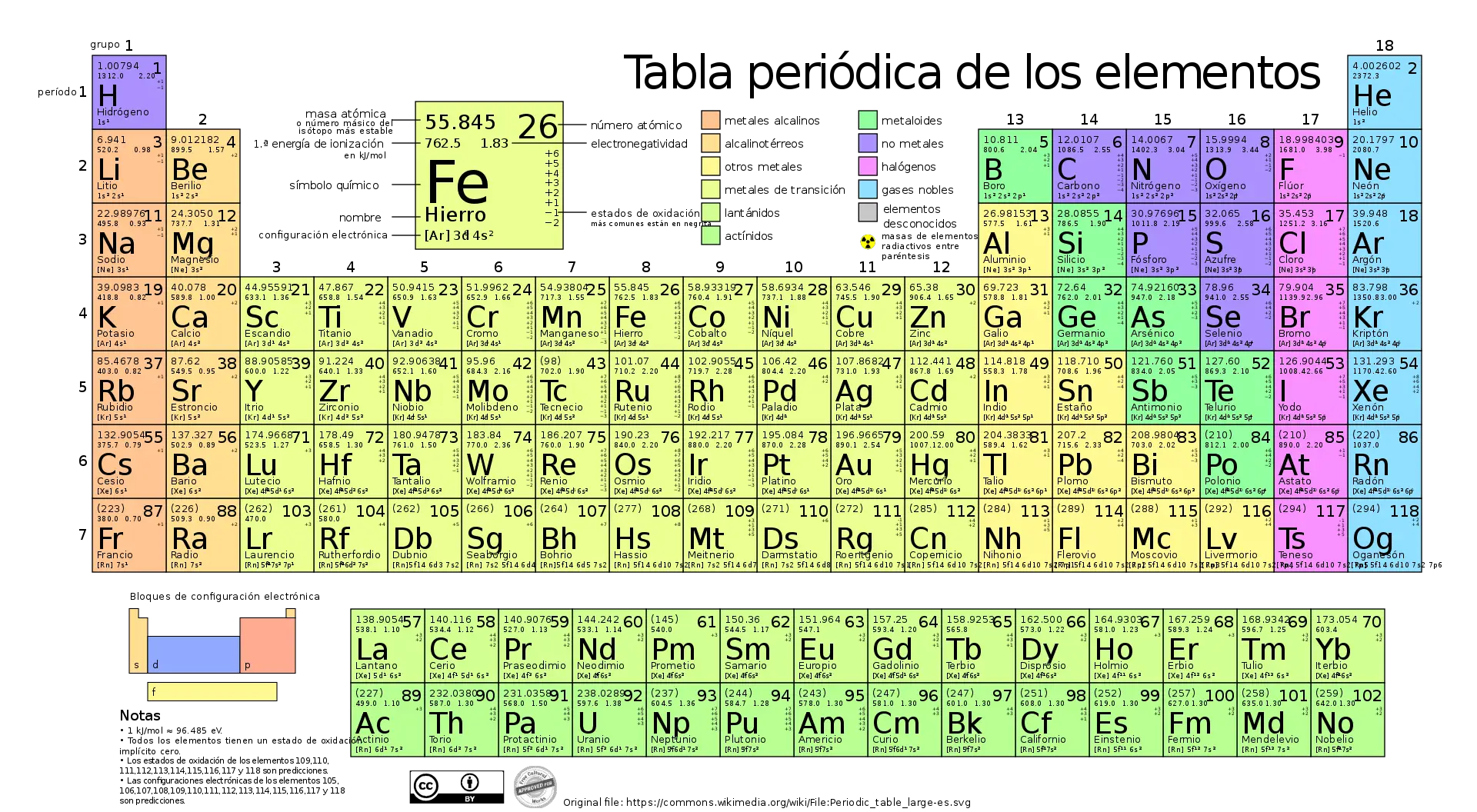 La tabla periódica moderna se basa en la estructura y organización propuesta por Mendeléyev, pero ha evolucionado con el tiempo a medida que se han descubierto más elementos y se ha avanzado en la comprensión de la estructura atómica y las propiedades químicas.
La tabla periódica moderna se basa en la estructura y organización propuesta por Mendeléyev, pero ha evolucionado con el tiempo a medida que se han descubierto más elementos y se ha avanzado en la comprensión de la estructura atómica y las propiedades químicas.
En la tabla periódica actual, los elementos se organizan en función de su número atómico, que es el número de protones en el núcleo de un átomo. Esto resulta en una organización que muestra claramente la periodicidad de las propiedades químicas de los elementos.
Las filas horizontales, llamadas períodos, representan niveles de energía en los que los electrones pueden encontrarse, y las columnas verticales, llamadas grupos, tienen elementos con propiedades químicas similares debido a su configuración electrónica similar.
Conclusiones
La ley de las octavas fue un intento temprano y valioso de organizar los elementos químicos, pero tenía limitaciones importantes y no podía explicar adecuadamente la organización de todos los elementos.
Fue la tabla periódica de Mendeléyev la que finalmente superó estas limitaciones y se convirtió en la herramienta esencial que conocemos hoy en día.
La organización de los elementos en la tabla periódica moderna se basa en el número atómico y refleja de manera precisa la periodicidad de las propiedades químicas de los elementos, lo que ha sido fundamental para avanzar en la química y la comprensión de la materia a nivel atómico.
En resumen, la ley de las octavas propuesta por Newlands fue un paso importante en este camino, pero solo fue el comienzo de un proceso continuo de descubrimiento y organización en la química.
